记住用户名密码
三氢化铝湿热稳定化的ALD钝化创新研究
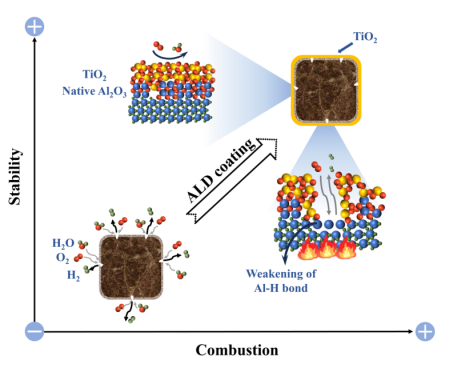
三氢化铝(AlH3)因其优异的储氢性能而备受关注,是固体推进剂中极好的金属基燃料。AlH3表面有一层天然的Al2O3氧化层,但这层氧化层表面通常伴随着一些孔洞和裂纹缺陷,在长期储存或者具体成药过程中,外界水氧会通过这些缺陷进入AlH3内部,从而发生释氢反应,导致能量下降,进而阻碍了其实际应用。
针对上述问题,华中科技大学陈蓉课题组采用原子层沉积技术(ALD),成功在AlH3表面开发低温沉积超薄TiO2薄膜工艺,且薄膜沉积厚度纳米可控,每循环TiO2的包覆仅带来0.0026 wt%的氢损失。包覆30循环TiO2(2.4 nm)的AlH3分解温度峰值为208.97 ℃,分解活化能为112.39 kJ mol-1,分别比裸样AlH3高7.83 ℃与25.62 kJ mol-1。水热老化条件下,TiO2包覆AlH3的氢含量损失远低于AlH3,这是由于在AlH3表面构建的Al2O3-TiO2双核壳薄膜结构有效修饰了原颗粒表面缺陷,实现钝化效果。同时,与裸样AlH3相比,TiO2包覆后的AlH3的燃烧性能增强,火焰辐射强度更强。根据密度泛函理论计算表明,在高温下,AlH3与TiO2的接触可以减弱Al-H离子键的强度,促进氢的释放。本工作为同时提高AlH3的稳定性和能量释放提供了可行的方法。
相关成果“Catalytically ultrathin titania coating to enhance energy storage and release of aluminum hydride via atomic layer deposition”发表在《Chemical Engineering Journal》期刊上(DOI:https://doi.org/10.1016/j.cej.2024.155809)。硕士生胡志佳为第一作者,陈蓉教授、刘潇副教授为共同通讯作者。
本工作中,我们采用ALD方法,在AlH3表面实现低温纳米级TiO2包覆,在AlH3表面构建了Al2O3-TiO2双核壳薄膜结构。TiO2线性性良好,生长速率为0.08 nm/c,经计算,每循环TiO2薄膜的包覆仅使AlH3释氢0.0026 wt%(图1),相较于其他文献,本工作对AlH3的氢损失有明显优势。同时,随着TiO2包覆层数的增加,AlH3表面的吸附氧比例逐渐降低,这是由于TiO2的修饰作用。

如图2所示SEM与TEM图像,包覆前后AlH3的粒径并未改变,颗粒仍然呈现立方体结构。包覆后的AlH3表面呈现出厚度均匀的TiO2薄膜,且面扫结果如下图所示:Al-Ti-O均匀分布在颗粒表面,且各元素在颗粒处有明显的富集现象。

SEM图和EDS图
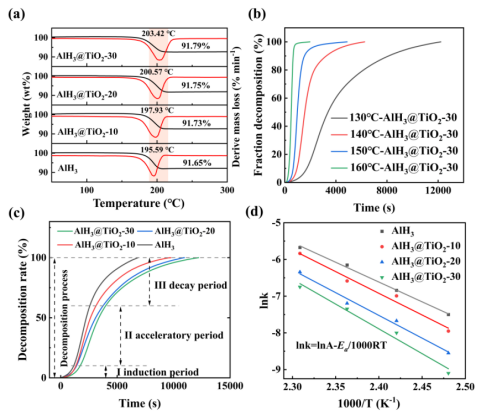
如图3(a)所示,包覆前后样品的ML值均在8.35 wt%左右,包覆后样品的ML值仅比AlH3低0.14%,与裸AlH3相比,AlH3@TiO2-30的Tp值提高了7.83 ℃,说明TiO2涂层可以明显提高AlH3的稳定性。同时,如图3(b-c)所示,同一样品的分解速率随着温度的升高而迅速增加,且AlH3表面TiO2薄膜越厚,分解速率越慢。如图3(d)所示,包覆样品的lnk值低于裸样AlH3,说明AlH3的活性高于包覆样品。且计算得到的AlH3与AlH3@TiO2-30的分解活化能数值分别为86.77 kJ mol-1与112.39 kJ mol-1,本方法达到的热稳定性能优于其他方法。
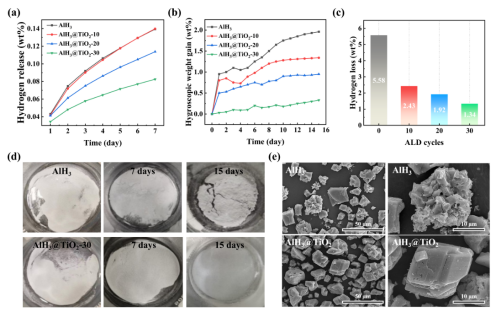
如图4所示,包覆TiO2的AlH3在真空条件下与湿热条件下的稳定性均得到提高,25 ℃、85%RH老化15天后,AlH3@TiO2-30的总增重仅为0.33 wt%,比AlH3 (1.96 wt%)低1.63wt%。且在老化过程中,由于H2O和O2的侵蚀,AlH3粉末颗粒发生团聚,而包覆后的样品老化后仍呈现松散状态,说明TiO2包覆层可以减缓H2O的侵蚀。
为了进一步研究AlH3的燃烧性能,激光点火过程和样品的相关火焰图像如图5所示。可以观察到AlH3的燃烧阶段与AlH3@TiO2-30粉末相同,表现为爆炸性燃烧。整个燃烧过程可以分为三个阶段:氢焰、延续和二次燃烧。在整个燃烧过程中,AlH3@TiO2-30样品的火焰明显比AlH3原料的火焰亮,这可能是TiO2膜对AlH3的催化活性使然。
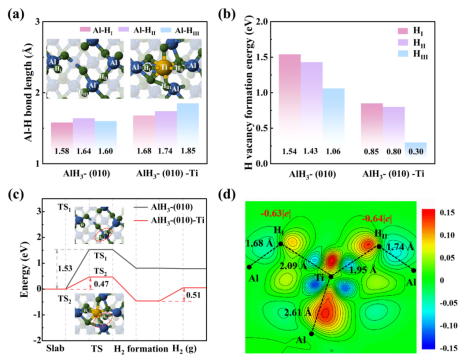
通过DFT计算研究了TiO2涂层增强AlH3燃烧性能的机理。为了模拟燃烧过程中TiO2与AlH3的直接接触,优化了由AlH3(010)板和吸附的Ti原子组成的原子模型,记为AlH3-(010)-Ti。如图6(a)所示,与AlH3-(010)- Ti相比,AlH3-(010)- Ti表面氢原子(HI、HII和HIII)与Al之间的键长被拉长。此外,Al-HII和Al-HIII的键长分别为1.74 Å和1.85 Å,比AlH3体中的Al-H键长1.72 Å。AlH3-(010)和AlH3-(010)- Ti上HI、HII和HIII的氢空位形成能如图6(b)所示,。由于Ti原子附近的Al-H键被拉伸,氢空位形成能明显低于AlH3-(010),表明Al-H离子键减弱。此外,AlH3-(010)和AlH3-(010)- Ti表面H2释放的能量路径如图6(c)所示。AlH3-(010)- Ti的H2生成能垒仅为0.47 eV,远低于AlH3-(010)的1.53 eV。虽然形成的H2分子在Ti原子上的化学吸附,但解吸势垒仅为0.51 eV,表明AlH3-(010)-Ti上的氢释放能力增强。图6(d)中AlH3-(010)-Ti上HI和HII原子截面的电荷密度差显示出表面氢原子和Ti原子之间明显的电荷聚集。HI和HII AlH3-(010)- ti的Bader电荷比AlH3-(010)的Bader电荷小,对应于拉伸的Al-H键。因此,我们可以得出结论,Ti和H之间的强电子相互作用可以减弱Al-H的结合强度,这有利于H2在高温下的快速释放。
总结展望:
我们开发了一种策略,利用ALD技术在AlH3表面包覆超薄TiO2涂层,通过改变TiO2包覆的ALD循环可以控制AlH3中氢含量的降低。AlH3@TiO2-30与裸AlH3相比,不仅表现出更强的热稳定性,而且由于TiO2涂层在燃烧过程中的催化能力,燃烧性能也得到了改善。涂覆TiO2后材料的稳定性能与能量释放性能的均增强是由于在AlH3表面形成了由惰性Al2O3和催化TiO2涂层组成的双壳状涂层结构,同时减缓了AlH3分解诱导期氢原子的扩散,加速了高温下H2的释放。我们的工作为同时提高AlH3的稳定性和能量性能提供了一种有效的方法。